글자크기 설정
기사의 본문 내용은 이 글자크기로 변경됩니다.
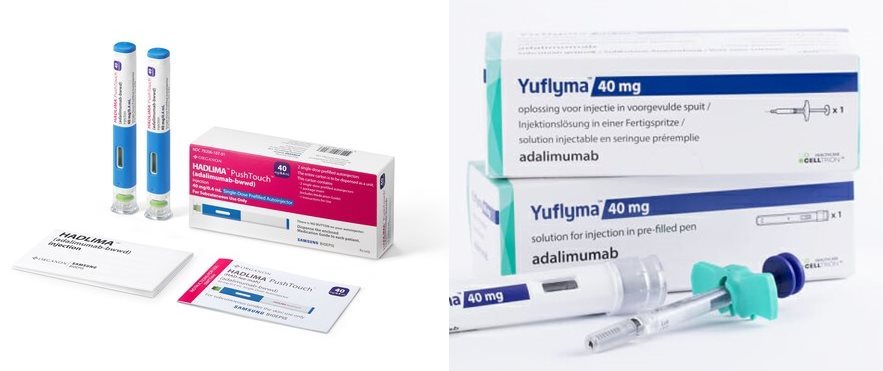
삼바에피스와 셀트리온헬스케어는 지난 7월 각각 휴미라의 바이오시밀러인 '하드리마'와 '유플라이마'를 휴미라의 최대 시장인 미국에 출시하며 경쟁에 뛰어들었다.
미국에서는 바이오시밀러 제품의 경우, 품목 허가와 별도로 제품의 상호교환성을 입증 받아야 약국에서의 대체조제가 가능하다. 이에 삼바에피스와 셀트리온헬스케어는 품목 허가에서 더 나아가 상호교환성 인증을 위한 절차를 밟았다.
그중 삼바에피스가 먼저 미국 내 환자들에게 접근성을 높이기 위한 목적으로 '하드리마'에 대한 미국 식품의약국(FDA)의 상호교환성 인증 관련 바이오의약품 변경 허가를 신청했고, 최근 하드리마의 상호교환성 임상을 모두 마무리 지은 뒤, 본격 심사 절차에 돌입했다.
하드리마가 이 심사에서 최종적으로 허가를 받을 경우, 미국에서 신규 환자가 아닌 휴미라를 사용하는 기존 환자들을 대상으로도 제품을 사용할 수 있어 시장을 더 크게 확대할 수 있을 것으로 예상된다.
경쟁사인 셀트리온헬스케어는 아직 유플라이마의 상호교환성 인증을 위한 임상 3상을 진행 중인 단계다.
이에 삼바에피스가 먼저 하드리마의 상호교환성 인증을 받게 되면 미국 휴미라 바이오시밀러 시장에서 셀트리온헬스케어보다 유리한 입지를 선점할 수 있을 것으로 보인다.
한편, 하드리마와 유플라이마의 오리지널 의약품인 휴미라는 류마티스 관절염, 소아 특발성 관절염 등에 처방된다.
이 기사를 공유합니다
조해진 기자
jhj@medipana.com

