이들 성분의 연간 청구액만 약 1700억원에 달해 국내 제약업계 내 일대 파란이 예상된다.
건강보험심사평가원은 4일 '2024년 건강보험약제 급여적정성 재평가' 심의 결과를 공개했다.
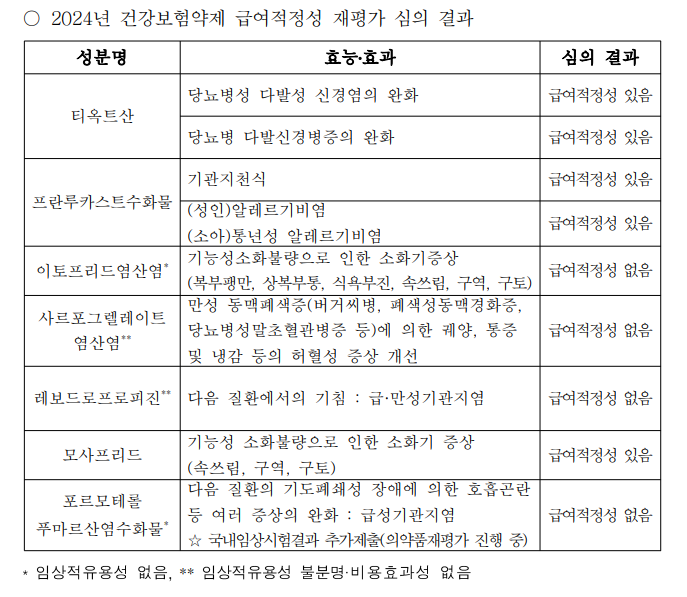
이들은 선정기준 및 전문가 자문 등을 통해 1998년부터 2001년 사이에 등재된 성분이다.
또 식약처에서 임상재평가 중인 성분으로써 임상적 유용성 등에 대한 재검토 필요성이 제기된 바 있다.
심의 결과, 사르포그렐레이트염산염과 레보드로프로피진, 이토프리드염산염, 프로모테롤 푸마르산염수화물 등 4종은 급여적정성이 없다고 결론지었다.
사르포그렐레이트염산염과 레보드로프로피진, 프로모테롤 푸마르산염수화물은 임상적 유용성이 불분명한데다 비용효과성이 없다는 판단이다. 이토프리드염산염은 아예 임상적 유용성이 없다고 평가받았다.
업계에 따르면 이들 성분약들의 최근 3년 연간 청구액은 1700억원에 달한다. 사르포그렐레이트염산염의 연간 청구액은 약 1100억원, 레보드로프로피진은 약 320억원, 이토프리드염산염은 약 240억원, 프로모테롤 푸마르산염수화물은 약 30억원 수준이다.
그런 만큼 급여 삭제가 이뤄지면, 해당 품목을 가진 제약사들로선 매출 공백이 불가피하다.
이와 함께 폐색성 비대성 심근병증 치료 신약인 한국BMS제약 '캄지오스(마바캄텐)'는 약평위를 통과했다.
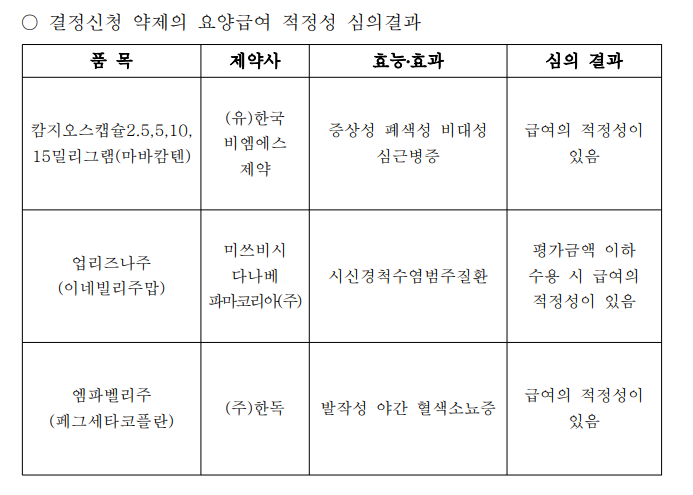
발작성 야간 혈색소뇨증 치료제 한독 '엠파벨리주(페그세타코플란)'도 약평위를 통과했다. 시신경척수염범주질환 치료제인 미쓰비시다나베파마코리아 '업리즈나주(이네빌리주맙)'는 평가금액 이하 수용 시에만 급여 적정성이 있다고 평가 받았다.
한편 7개 성분 관련 제약사는 결과통보 후 30일 이내에 이의신청서를 심평원에 제출할 수 있으며, 제출된 내용은 약평위의 재심의를 거치게 된다.

