
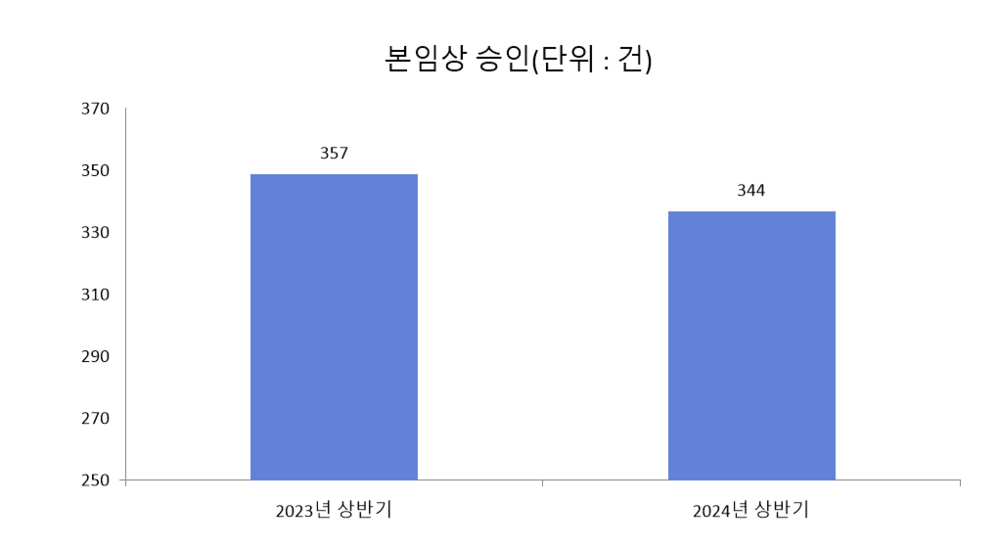
1일 메디파나뉴스가 취합한 통계에 따르면, 식품의약품안전처가 올해 상반기에 승인한 임상은 499건으로, 전년 556건 대비 10.3% 감소했다. 특히 연구자 임상과 생동을 제외한 본임상 승인은 344건으로 전년 357건 대비 3.6% 감소했다.
그는 "최근 의료계와 정부 사이에 갈등이 있는데, 그것 때문에 임상을 늦추거나 그런 부분은 없다"며 "전임상에서 본임상에 들어갈 만한 후보군을 추리는 과정을 거치다 보니 조금 줄어든 게 있는 것 같다"고 설명했다.
B 제약사 관계자는 외부 환경 변화가 임상 진행 과정에 큰 영향을 주지 않았다고 일축했다. 그는 "상반기에 발생한 의료계 이슈에 대해 문의를 많이 받았는데, 관련 부서에 확인해 보니 영향이 미미하다는 답이 돌아왔다"고 밝혔다.
이어 "매년 매출액 일정 비율 이상 의약품 연구개발에 투자하는 상황에서, 본임상 단계에 따라 탄력적으로 운영하는 건 있다"며 "최근 이슈 영향으로 임상을 승인받지 못한 건 전혀 없다"고 덧붙였다.
C 제약사 관계자도 A, B 제약사 관계자와 비슷한 답변을 내놨다. 그는 최근 의·정 갈등 상황에서 임상 계획을 변경한 게 있는지 묻는 말에 "저희랑 크게 관련이 없어 보인다"고 시큰둥한 반응을 보였다.
올해 상반기 연구자 임상 및 생동 승인은 본임상과 다른 모습이 나타났다. 식약처가 지난 1·2분기에 승인한 연구자 임상 및 생동은 각각 46건, 109건으로 지난해 같은 기간과 비교해 19.3%, 23.2%가량 줄었다.
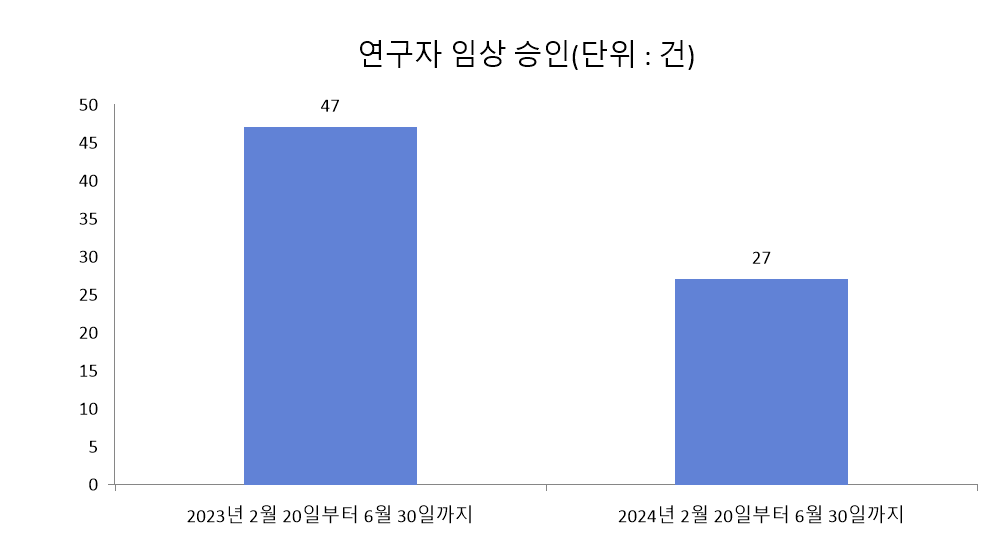
식약처 자료에 따르면, 빅5 병원 전공의가 사직서를 제출한 다음 날(2월 20일)부터 지난달 30일까지 연구자 임상 승인 건수는 27건으로, 전년 동기 대비 약 42.6% 줄었다.
최근 D 상급종합병원 교수는 메디파나뉴스와 통화에서 "기존 임상에선 환자 모집 기간을 길게 가져가면 문제는 없겠지만, 신규 임상은 승인도 어렵고 승인을 받더라도 당장 진행이 되겠나"라고 말한 바 있다.
그는 "교수들이 당직 근무까지 서야 하는 상황에서 사실상 정상적인 임상 진행이 힘들다고 본다"며 "의료 공백 장기화 해결 실마리가 없다면, 당분간 임상 연구 활동에 차질이 불가피할 것"이라고 전망했다.
한편, 국내 제약업체 중 올해 상반기에 가장 많은 임상을 승인받은 기업은 유한양행 신약 개발 자회사 애드파마다. 식약처는 지난 1·2분기에 고혈압 환자에 처방하는 복합제 'AD-209' 3상 등 임상 15건을 승인했다.
애드파마 뒤를 이은 국내 업체는 제뉴파마다. 해당 기업이 올해 상반기에 승인받은 임상은 9건이다. 식약처는 당뇨 복합제 'GNS-20I04-1' 1상, 복합형 이상지질혈증 치료제 'GNS-214-C' 1상 등 시험을 승인했다.

