
9일 업계에 따르면, 최근 대원제약은 식품의약품안전처로부터 'DW5124' 임상 1상을 승인받았다. 이번 1상은 건강한 성인 자원자를 대상으로 DW5124와 DW5124-R 안전성, 약동학적 특성과 음식물이 DW5124에 미치는 영향을 평가하기 위한 시험이다.
정부 자료에 따르면, DW5124는 피타바스타틴 2mg 단일 투여 시 LDL-콜레스테롤 수치를 조절할 수 있으나, 트리글리세라이드 수치가 높고 HDL-콜레스테롤 수치가 낮은 복합형이상지질혈증(관상동맥심질환(CHD) 고위험 성인)에 쓰인다.
이번 임상은 대원제약이 순환기(심혈관)계 연구개발(R&D)에 공들이는 모습을 보여준다. 대원제약은 지난해 하반기에 원발성 고콜레스테롤혈증 또는 혼합형 이상지질혈증 치료에 사용하는 'DW-5421' 3상에 진입한 바 있다.
아울러 비슷한 시기에 원발성 고콜레스테롤혈증 치료제 '리토젯정10/5mg(에제티미브,아토르바스타틴칼슘삼수화물)'을 출시했으며, 지난해 12월 들어 본태성 고혈압 복합제 'DW-2222' 생동을 식약처에서 승인받았다.
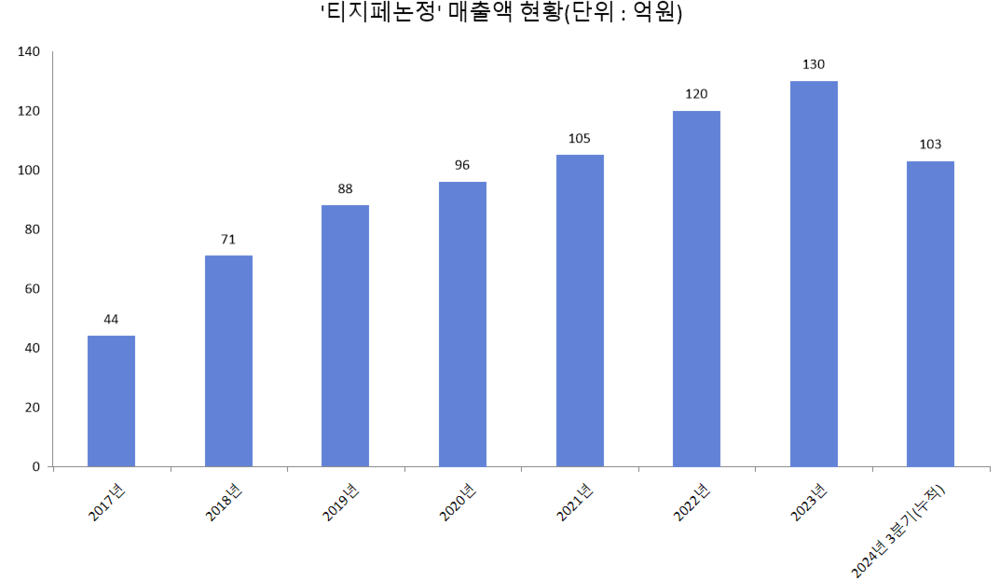
공시 자료에 따르면, 티지페논정 매출액은 출시 첫해인 2017년 44억원에서 지난해 130억원으로 3배 가까이 늘었다. 연평균 증가율로 환산하면, 매출액이 6년간 매년 20%가량 증가한 셈이다.
매출액 증가세는 최근까지 이어졌다. 대원제약은 분기 보고서에서 티지페논정 지난해 3분기(누적) 매출액이 전년 동기 대비 4.2% 늘어난 103억원이라고 밝혔다. 타지페논정 매출액이 3분기 만에 100억원을 넘은 건 지난해가 처음이다.
이상지질혈증 치료제 '타바로젯정(피타바스타틴칼슘, 에제티미브)'도 순환기계 성과를 보여주는 품목이다. 해당 품목은 대원제약이 JW중외제약 '리바로젯' 제네릭으로 개발 후 2023년 국내 시장에 내놓은 의약품이다.
대원제약은 최근 실적 발표 자료에서 의약품 시장 조사기관 유비스트(UBIST) 자료를 근거로 타바로젯정 원외처방실적(누적)이 100억원을 넘었다고 밝혔다. 이는 해당 품목을 출시한 지 1년여 만에 달성한 성과다.
이 회사는 이런 성과를 바탕으로 전체 품목 원외처방실적에서 심혈관계 비중을 일정 수준으로 유지하고 있다.
최근 실적 발표 자료에 따르면, 대원제약 질환별 원외처방실적에서 심혈관계 품목이 차지하는 비중은 2019년과 2020년에 20.5%, 23.1%로 나타났으며, 2022년과 2023년에 각각 19.2%, 18.6%로 집계됐다.

