[메디파나뉴스 = 박으뜸 기자] 제약업계의 관심을 모았던 천연물신약 급여 재평가에서 희비가 엇갈렸다.
'위령선·괄루근·하고초'는 급여 적정성을 인정받았지만, '애엽 추출물'은 탈락했다.
건강보험심사평가원이 발표한 2025년 재평가 대상 성분은 ▲올로파타딘염산염 ▲위령선·괄루근·하고초 ▲베포타스틴 ▲구형흡착탄 ▲애엽추출물 ▲L-오르니틴-L-아스파르트산 ▲설글리코타이드 ▲케노데속시콜산-우르소데속시콜산삼수화물마그네슘염 등 총 8개다.
이 중 위령선·괄루근·하고초, 애엽 추출물 등 천연물 기반 성분이 포함돼, 특히 국산 천연물 신약을 개발해온 제약사들의 반발이 거셌다.
그러나 심평원은 재평가 약제 선정은 '국산 여부'가 아니라 사전에 고시된 기준에 따른 절차라는 입장이다.
최근 전문기자단 간담회에서 심평원 약제관리실은 "재평가 대상은 선정기준에 해당하는 모든 약제를 대상으로 하며, 성분의 원개발국가를 고려해 선정하고 있지 않다"고 밝히 바 있다. 이번에 포함된 천연물 신약들이 평가 대상으로 선정되더라도 임상적 유용성이 인정되면 급여는 유지된다는 것이다.
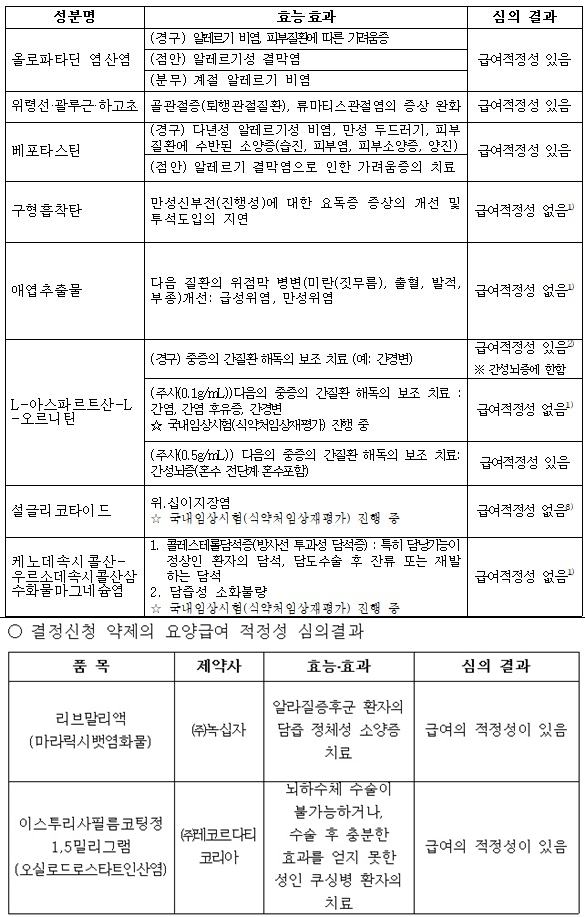
심평원이 7일 발표한 '제8차 약제급여평가위원회' 심의 결과에 따르면 ▲올로파타딘염산염은 (경구) 알레르기 비염, 피부질환에 따른 가려움증, (점안) 알레르기성 결막염, (분무) 계절성 알레르기 비염 치료 ▲위령선·괄루근·하고초는 골관절증(퇴행관절질환), 류마티스관절염의 증상 완화 ▲베포타스틴은 (경구) 다년성 알레르기성 비염, 만성 두드러기, 피부질환에 수반된 소양증(습진, 피부염, 피부소양증, 양진), (점안) 알레르기 결막염 치료 ▲L-아스파르트산-L-오르니틴은 (경구) 중증 간질환 해독의 보조 치료 및 간성뇌증에, (주사, 0.5g/mL) 간성뇌증(혼수 전단계 및 혼수 포함)에 대해 급여 적정성이 있다고 판단됐다.
반면 ▲구형흡착탄은 만성신부전(진행성)에 따른 요독증 증상 개선 및 투석 도입 지연 ▲애엽추출물은 급성위염·만성위염에 동반된 위점막 병변(미란, 출혈, 발적, 부종) 개선 ▲L-아스파르트산-L-오르니틴(주사, 0.1g/mL)은 간염, 간염 후유증, 간경변 등 중증 간질환 해독의 보조 치료 ▲설글리코타이드는 위·십이지장염 ▲케노데속시콜산-우르소데속시콜산삼수화물마그네슘염은 콜레스테롤 담석증 및 담즙성 소화불량에 대해 심의가 이뤄졌지만, 급여 적정성은 인정되지 않았다.
구형흡착탄, 애엽추출물, L-아스파르트산-L-오르니틴(저용량 주사제), 케노데속시콜산-우르소데속시콜산삼수화물마그네슘염의 경우, 임상적 유용성을 뒷받침할 근거가 부족하다는 이유였다. 설글리코타이드는 임상적 유용성이 불분명하고, 비용 효과성도 낮다는 점이 판단 근거였다.
재평가 대상 성분의 제약사는 결과 통보 후 30일 이내에 건강보험심사평가원에 이의신청서를 제출할 수 있으며, 신청 내용은 약제급여평가위원회의 재심의를 거치게 된다.
한편 이번 회의에서는 GC녹십자의 '리브말리액(마라릭시뱃염화물)'과 레코르다티코리아의 '이스투리사필름코팅정 1.5밀리그램(오실로드로스타트인산염)'에 대한 급여 적정성 심의도 진행됐다.
리브말리액은 '알라질증후군 환자의 담즙 정체성 소양증 치료'에, 이스투리사는 '뇌하수체 수술이 불가능하거나, 수술 후 충분한 효과를 얻지 못한 성인 쿠싱병 환자 치료'에 대해 급여 적정성이 인정됐다.

